REVIEW
HDVR 2024, 35(4): 215-225
VIN (Vulvar Intraepithelial Neoplasia)
Despina Exadaktilou
Dermatologist – Venereologist, Clinical Director
Dermatology Department General Hospital “Agia Varvara” – General Hospital “Agios Panteleimon”
ABSTRACT
Vulvar intraepithelial neoplasia (VIN) is a precursor of squamous cell carcinoma (SCC) of the vulva and is classified into:
1. Vulvar low-grade squamous intraepithelial lesions (vL-SIL).
2. High-grade vulvar lesions, further divided into:
2a. Vulvar high-grade squamous intraepithelial lesions (vH-SIL) and
2b. Differentiated Vulvar Intraepithelial Neoplasms (dVIN)
The diagnosis is made by histological examination and immunohistochemistry, and multiple samples are required in multifocal lesions. There is lack of evidence based criteria and discrepancy in the literature for the treatment of VIN. The 2016 European guideline for differentiated intraepithelial neoplasia (dVIN) recommends surgical excision as the treatment of choice with margins of at least 5mm and regular post-treatment follow up. For high-grade squamous intraepithelial lesions of the vulva (vH-SIL), surgical removal and Co2 Laser are traditionally recommended, but the increased frequency of recurrences and the psychological burden they entail has led to recommendation of medical treatments such as topical imiquimod. Recently, the option of “wait and see” has been gaining ground, especially in younger patients in whom spontaneous regression has been observed. HPV vaccination is thought to be preventative and will reduce the incidence of vL-SIL and vH-SIL.
ΠΕΡΙΛΗΨΗ
H Ενδοεπιθηλιακή νεοπλασία του αιδοίου (VIN) θεωρείται πρόδρομο στάδιο του ακανθοκυτταρικού καρκινώματος (ΑΚΚ) του αιδοίου και διαχωρίζεται σε:
1. Χαμηλού βαθμού πλακώδεις ενδοεπιθηλιακές βλάβες του αιδοίου (vulvar low-grade squamous intraepithelial lesions: vL-SIL).
2. Υψηλού βαθμού βλάβες του αιδοίου (High-grade vulvar lesions), οι οποίες διαχωρίζονται περαιτέρω σε:
2α. Υψηλού βαθμού πλακώδεις ενδοεπιθηλιακές βλάβες του αιδοίου (Vulvar high-grade squamous intraepithelial lesions: vH-SIL) και
2β. Διαφοροποιημένες ενδοεπιθηλιακές νεοπλασίες του αιδοίου (Differentiated Vulvar Intraepithelial Neoplasms: dVIN)
Η διάγνωση τίθεται με την ιστολογική εξέταση και την ανοσοϊστοχημεία και σε πολυεστιακές βλάβες απαιτούνται πολλαπλά δείγματα. Για τη θεραπεία της VIN υπάρχει έλλειψη τεκμηριωμένων κριτηρίων και ασυμφωνία στη βιβλιογραφία. Η ευρωπαϊκή κατευθυντήρια γραμμή του 2016 για τη διαφοροποιημένη Ενδοεπιθηλιακή Νεοπλασία (dVIN) συστήνει τη χειρουργική εκτομή ως θεραπεία εκλογής με όρια υγιούς ιστού τουλάχιστον 5mm και τακτική παρακολούθηση μετά τη θεραπεία. Για την υψηλού βαθμού πλακώδη ενδοεπιθηλιακή βλάβη του αιδοίου (vH-SIL) παραδοσιακά αναφέρονται η χειρουργική αφαίρεση και η εξάχνωση με Co2 Laser αλλά η αυξημένη συχνότητα υποτροπών και η ψυχολογική επιβάρυνση που συνεπάγονται έχει οδηγήσει στη σύσταση συντηρητικής θεραπείας όπως η τοπική χορήγηση ιμικουϊμόδης. Τελευταία κερδίζει έδαφος η αναμονή & παρακολούθηση (wait and see) ιδιαίτερα σε νεότερες ασθενείς στις οποίες έχει παρατηρηθεί και αυτόματη υποστροφή. Ο εμβολιασμός έναντι των HPV θεωρείται ότι δρα προληπτικά και θα μειώσει τη συχνότητα εμφάνισης των vL-SIL και vH-SIL.
Keywords: Low grade intraepithelial neoplasia, high grade intraepithelial neoplasia, differentiated intraepithelial neoplasia, HPV
Corresponding author: Δέσποινα Εξαδακτύλου, email: despgr@hotmail.com
ΕΝΔΟΕΠΙΘΗΛΙΑΚΗ ΝΕΟΠΛΑΣΙΑ ΤΟΥ ΑΙΔΟΙΟΥ (VIN)
Α. Ταξινόμηση
Η ταξινόμηση της ενδοεπιθηλιακής νεοπλασίας του αιδοίου (VIN) στη βιβλιογραφία, έχει υποστεί πολλές αλλαγές από τότε που περιγράφηκε για πρώτη φορά πριν από σχεδόν 100 χρόνια.
Η τρέχουσα ορολογία του κατώτερου γεννητικού συστήματος (Lower Anogenital Squamous Terminology: LAST) η οποία αναπτύχθηκε από τη Διεθνή Εταιρεία για τη Μελέτη των Παθήσεων του Αιδοίου (International Society for the Study of Vulvar Disease: ISSVD) διαχωρίζει τις πλακώδεις βλάβες του πρωκτογεννητικού συστήματος της γυναίκας σε:
1. Χαμηλού βαθμού πλακώδεις ενδοεπιθηλιακές βλάβες του αιδοίου (vulvar low-grade squamous intraepithelial lesions: vL-SIL). Αυτή η κατηγορία περιλαμβάνει καλοήθεις αλλοιώσεις που σχετίζονται με λοίμωξη από χαμηλού κινδύνου στελέχη του ιού των ανθρώπινων κονδυλωμάτων (human papillomavirus: HPV).
2. Υψηλού βαθμού βλάβες του αιδοίου (High-grade vulvar lesions), οι οποίες επηρεάζουν μεταξύ 2,5 και 8,8 ανά 100.000 γυναίκες και διαχωρίζονται περαιτέρω σε:
2α. Υψηλού βαθμού πλακώδεις ενδοεπιθηλιακές βλάβες του αιδοίου (Vulvar high-grade squamous intraepithelial lesions: vH-SIL), παλαιότερα γνωστές ως συνήθης τύπος VIN (VIN usual type). Οι βλάβες αυτές σχετίζονται με λοίμωξη από υψηλού κινδύνου στελέχη HPV και μπορούν να εξελιχθούν σε διηθητικό καρκίνο του αιδοίου.
2β. Διαφοροποιημένες ενδοεπιθηλιακές νεοπλασίες του αιδοίου (Differentiated Vulvar Intraepithelial Neoplasms: dVIN), οι οποίες αναπτύσσονται σε υποκείμενες χρόνιες δερματικές βλάβες (κυρίως σε έδαφος σκληροατροφικού λειχήνα) και έχουν μεγαλύτερη πιθανότητα κακοήθους εξαλλαγής1-2.
Η παραπάνω ταξινόμηση είναι με βάση την ιστολογική εικόνα των βλαβών και σε αυτές τις κατηγορίες υπάγονται οι αντίστοιχες κλινικές παθήσεις.
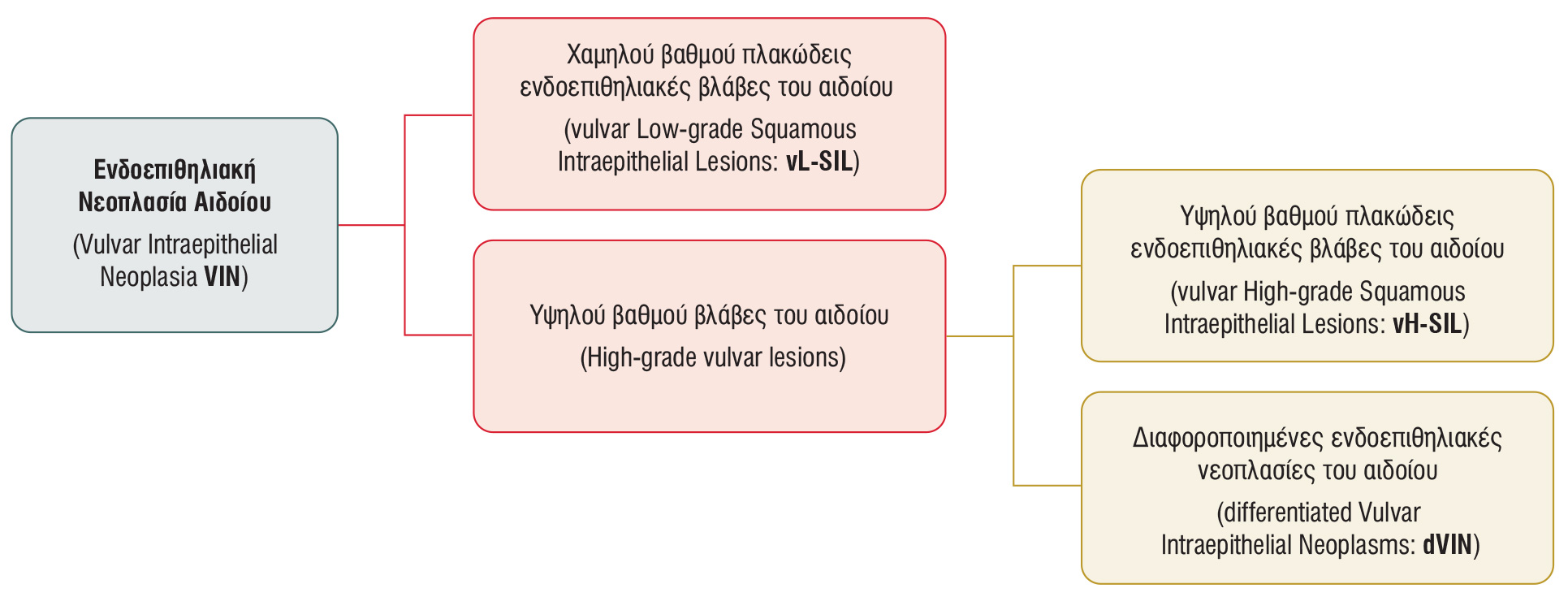
ΣΧΗΜΑ 1. Ταξινόμηση της ενδοεπιθηλιακής νεοπλασίας του αιδοίου (VIN) κατά την ορολογία του κατώτερου γεννητικού συστήματος (Lower Anogenital Squamous Terminology: LAST) της Διεθνούς Εταιρείας για τη Μελέτη των Παθήσεων του Αιδοίου (International Society for the Study of Vulvar Disease: ISSVD).
1. Χαμηλού βαθμού πλακώδης ενδοεπιθηλιακή βλάβη του αιδοίου- Vulvar low-grade squamous intraepithelial lesions (vL-SIL)
Κλινικά, στην κατηγορία αυτή περιλαμβάνονται δύο τύποι χαμηλού βαθμού πλακώδους ενδοεπιθηλιακής βλάβης του αιδοίου (vL-SIL):
- Τα οξυτενή κονδυλώματα και
- Ο όγκος Buschke-Lowenstein
Οι βλάβες αυτές σχετίζονται με λοίμωξη από χαμηλού κινδύνου στελέχη HPV (6 ή 11 σχεδόν στο 90% των περιπτώσεων) και δεν εξελίσσονται σε διηθητικό καρκίνο. Εξαίρεση αποτελούν κάποιοι όγκοι Buschke-Lowenstein, οι οποίοι είναι σπάνιοι στις γυναίκες, στους οποίους έχουν ανιχνευτεί στελέχη ογκογόνων τύπων HPV, συμπεριλαμβανομένων των HPV 16 και HPV 183.
Ο HPV μεταδίδεται μέσω άμεσης επαφής και η μολυσματική επαφή είναι υπεύθυνη για το 60% έως 70% όλων των περιπτώσεων των πρωκτογεννητικών κονδυλωμάτων. Οι συν-παράγοντες κινδύνου περιλαμβάνουν το κάπνισμα και την ανοσοκαταστολή (CD4+ Τ κύτταρα <200/mm3)2.
2. Υψηλού βαθμού βλάβες του αιδοίου (High-grade vulvar lesions), οι οποίες διαχωρίζονται σε:
2α. Υψηλού βαθμού πλακώδεις ενδοεπιθηλιακές βλάβες του αιδοίου (Vulvar high-grade squamous intraepithelial lesions: vH-SIL)
παλαιότερα γνωστές ως συνήθης τύπος VIN (VIN usual type). Οι βλάβες αυτής της κατηγορίας συνδέονται άμεσα με λοίμωξη από HPV υψηλού κινδύνου. Μια πρόσφατη μετα-ανάλυση ανέφερε επιπολασμό HPV 86,2% για τη vH-SIL (356 περιπτώσεις από 10 μελέτες) σε σύγκριση με μόλις 2,0% για τη dVIN με παρόμοια κατανομή των γονότυπων και στις δύο ομάδες. Οι πιο συνηθισμένοι τύποι HPV οι οποίοι αναφέρονται στη βιβλιογραφία ότι εμπλέκονται στις vH-SIL είναι ο HPV 16 (77,2%), HPV 33 (10,6%), HPV 18 (2,6%) και HPV 31 (1,2%). Οι παράγοντες κινδύνου για vH-SIL είναι οι κλασικοί παράγοντες που συνδέονται με βλάβες που σχετίζονται με λοίμωξη από τους ιούς HPV: οικογενειακή κατάσταση με αναλογία κινδύνου (hazard ratio HR 1,77), από του στόματος χρήση αντισυλληπτικών (HR 1,46), χρήση εμμηνοπαυσιακών ορμονών (HR 1,73) και κάπνισμα, το οποίο είχε το υψηλότερο HR στο 3,881.
Κλινικά, εμφανίζονται σε νεαρές ηλικίες (30-50 ετών) ως κηλίδες, βλατίδες και πλάκες, επηρμένες, χρώματος ερυθρού η/και καφεοειδούς ενώ μπορεί να είναι μελαγχρωματικές. Συνήθως παρατηρούνται πολλαπλές βλάβες, αμφοτερόπλευρα στο αιδοίο & περιπρωκτικά1,2. Πρόκειται, λοιπόν, για πολυεστιακή νεοπλασία και η πολυεστιακότητα αυτή εξαρτάται από τη ηλικία της ασθενούς καθώς μειώνεται από 59% σε γυναίκες ηλικίας 20-34 ετών σε 10% σε γυναίκες άνω των 50 ετών4.
Οι βλάβες στο 30% των ασθενών είναι ασυμπτωματικές αλλά στα 2/3 των περιπτώσεων προκαλούν διαλείποντα άλγος ή κνησμό1,4.
Κλινικά η διαφορική διάγνωση από τα οξυτενή κονδυλώματα είναι αδύνατη και η διάγνωση μπαίνει με την ιστολογική εξέταση της βλάβης.
Έχει περιγραφεί αυτόματη υποστροφή στο 1,2% των ασθενών οι οποίες ήταν όλες νεότερες των 35 ετών και συχνά σχετιζόταν με εγκυμοσύνη, παρουσιάζοντας συνήθως πολυεστιακές μελαγχρωματικές αλλοιώσεις4.
Ο κίνδυνος κακοήθους εξαλλαγής προς διηθητικό SCC σε 1-8 έτη χωρίς θεραπεία, σύμφωνα με μια μετα-ανάλυση αναφέρεται στο 8/88 (9%) ασθενών με vH-SIL ενώ σε άλλες μελέτες αναφέρεται πολύ υψηλότερο ποσοστό, 10/63 (15,8%) των ασθενών. Στις ασθενείς που έλαβαν θεραπεία, το ποσοστό εξαλλαγής κατά την παρακολούθηση μετά τη θεραπεία ήταν 3,3% (208/3322) και ο ρυθμός εξέλιξης δεν επηρεάστηκε από την έκταση της χειρουργικής επέμβασης. Μια πληθυσμιακή μελέτη από τη Νορβηγία έδειξε ότι τα όρια εκτομής δεν εμπόδισαν την εξέλιξη σε διηθητικό ΑΚΚ. Σε αυτή τη μελέτη, το 50% των ασθενών που ανέπτυξαν ΑΚΚ αιδοίου μετά τη θεραπεία είχαν ελεύθερα χειρουργικά όρια. Επομένως, οι εκτεταμένες χειρουργικές επεμβάσεις στη vH-SIL δεν προστατεύουν τις ασθενείς από την εμφάνιση ΑΚΚ4.
2β. Διαφοροποιημένες ενδοεπιθηλιακές νεοπλασίες του αιδοίου (Differentiated Vulvar Intraepithelial Neoplasms: dVIN)
Οι διαφοροποιημένες ενδοεπιθηλιακές νεοπλασίες του αιδοίου είναι σπάνιες και εμφανίζονται σε μεγαλύτερες ηλικίες (60-80 ετών). Συνήθως αναπτύσσονται σε έδαφος υποκείμενου σκληροατροφικού λειχήνα και στην αιτιοπαθογένειά τους εμπλέκονται το περιβάλλον χρόνιας φλεγμονής, το ισχαιμικό – οξειδωτικό στρες και οι μεταλλάξεις στο p531.
Οι HPV δεν σχετίζονται με dVIN και ο επιπολασμός τους σε αυτές τις βλάβες είναι αντίστοιχος με αυτόν του γενικού πληθυσμού παρόμοιας ηλικίας1,4.
Κλινικά παρουσιάζεται ως μονήρης, ετερόπλευρη, σαφώς αφοριζόμενη, ελαφρά επηρμένη, ερυθηματώδης πλάκα η οποία εντοπίζεται στα μεγάλα χείλη του αιδοίου. Οι ασθενείς συχνά αναφέρουν μακροχρόνιο ιστορικό συμπτωμάτων κνησμού και/ή καύσους του αιδοίου που σχετίζονται με τον υποκείμενο σκληροατροφικό λειχήνα1,4.
Η 10ετής αθροιστική επίπτωση του κερατινοποιημένου ΑΚΚ (keratinizing VSCC) αναφέρεται ότι αγγίζει το 18,8% σε γυναίκες με ταυτόχρονο σκληροατροφικό λειχήνα & dVIN, έναντι του 2,8% σε γυναίκες μόνο με σκληροατροφικό λειχήνα1.
Β. Μοριακή βιολογία
Η αιτιολογία της VHSIL σχετίζεται με HPV υψηλού κινδύνου (HPV 16 στο >70% των περιπτώσεων), κάπνισμα και ανοσοκαταστολή. Οι παθογενετικοί μηχανισμοί της ογκογένεσης της VHSIL περιλαμβάνουν σημαντικά επίπεδα μεθυλίωσης του DNA των κυττάρων του ξενιστή τα οποία αποτελούν ένδειξη υψηλού κίνδυνου κακοήθειας. Σε μελέτη ολόκληρου του γονιδιώματος παρατηρήθηκε ότι η αύξηση του χρωμοσώματος 1pq αποτελεί ισχυρό προγνωστικό παράγοντα για την εξέλιξη της HPV-θετικής VIN σε ΑΚΚ2.
Οι χρόνιες φλεγμονώδεις διαταραχές, όπως ο σκληροατροφικός ή ο ομαλός λειχήνας, είναι οι κύριες αιτίες της dVIN και του HPV-αρνητικού ΑΚΚ του αιδοίου. Οι μεταλλάξεις TP53 παρατηρούνται συνήθως σε ασθενείς με dVIN. Επιπλέον, σε HPV-αρνητική VIN (παρόμοια με το HPV-αρνητικό ΑΚΚ του αιδοίου), έχουν τεκμηριωθεί η κλωνική ενίσχυση D1 και οι μεταβολές του αριθμού αντιγράφων στα χρωμοσώματα 3, 8 και 11q132.
Ένας τρίτος, μέχρι στιγμής άγνωστος μοριακός υπότυπος έχει προταθεί με βάση την ανακάλυψη ότι ένα ποσοστό των προδιαθεσικών παραγόντων που είναι ανεξάρτητοι από τους ιούς HPV, είναι ο TP53 άγριου τύπου με σωματικές μεταλλάξεις στα PIK3CA, NOTCH1 και HRAS2.
Σύμφωνα με πρωτεομικές μελέτες, η φλεγμονή παίζει βασικό ρόλο στην πορεία του σκληροατροφικού και του ομαλού λειχήνα, όπου οι χρόνιες φλεγμονώδεις καταστάσεις πιστεύεται ότι είναι οι κύριες αιτίες οξειδωτικής βλάβης και τοπικής ανοσολογικής δυσλειτουργίας. Οι διαταραχές στο μικροβίωμα του αιδοίου και του κόλπου φαίνεται επίσης ότι προκαλούν φλεγμονώδη απόκριση, η οποία τροποποιεί την ισορροπία των κοινών μικροοργανισμών στον ξενιστή2.
Γ. Ανοσολογία
Η επίμονη λοίμωξη από HPV στην VHSIL, δημιουργεί ένα τοπικό ανοσοκατασταλτικό περιβάλλον με αυξημένη διήθηση από Τ-ρυθμιστικά κύτταρα (Tregs) και Τ βοηθητικά (CD4+) και μειωμένο αριθμό κυτταροτοξικών Τ κύτταρων (CD8+). Οι ασθενείς με μη υποτροπιάζουσα και υποτροπιάζουσα VHSIL διερευνήθηκαν για την παρουσία και την κλινική σημασία των τύπων των μυελοειδών κυττάρων. Η ομάδα της υποτροπιάζουσας VHSIL εμφάνισε τον υψηλότερο αριθμό ενδοεπιθηλιακών CD14+ (δείκτης μονοκυττάρων). Επίσης, ο πληθυσμός των Μ2 μακροφάγων στη VHSIL ήταν τουλάχιστον τέσσερις φορές μεγαλύτερος από αυτόν των Μ1 μακροφάγων, υποδεικνύοντας ένα ανοσοκατασταλτικό περιβάλλον εντός του επιθηλίου της VHSIL2.
Σε VHSIL, η κλινική ανταπόκριση στην ανοσοθεραπεία συνδέεται με μείωση του αριθμού των Treg και αύξηση των ενδοβλαβικών CD8+. Η ιστολογική υποχώρηση της VHSIL σχετίζεται με ομαλοποίηση του αριθμού των CD4+, CD8+ και Τ κυττάρων στην επιδερμίδα και την εξάλειψη του HPV. Η μείωση των ενδοεπιθηλιακών κυττάρων CD14+ και η αύξηση των κυττάρων CD1a+ και κυττάρων Langerhans συνδέθηκαν με την κάθαρση του HPV κατά τη διάρκεια της θεραπείας με ιμικουιμόδη για VHSIL. Αντίθετα η αύξηση των CD14+ και μυελοειδών κυττάρων υποδεικνύει προοδευτική εξαλλαγή προς ΑΚΚ του αιδοίου2.
Δ. Διάγνωση Ενδοεπιθηλιακής Νεοπλασίας Αιδοίου (VIN)
Η εξέταση των ασθενών με ύποπτες βλάβες του αιδοίου πρέπει να περιλαμβάνει:
- Λεπτομερή κλινική εξέταση όλης της περιοχής του αιδοίου και πρωκτού, και επιπλέον των μηροβουβωνικών λεμφαδένων και της ηβικής περιοχής.
- Γυναικολογική εξέταση κόλπου – τραχήλου μήτρας.
- Τεστ Παπανικολάου τραχήλου και πρωκτού.
- Ανάλογα με τις σεξουαλικές πρακτικές της ασθενούς επιπλέον εξέταση σε άλλες ανατομικές περιοχές όπως τα ώτα, η ρίνα και η στοματική κοιλότητα1.
- Η δοκιμασία οξικού οξέος δε συστήνεται λόγω υψηλού ποσοστού ψευδώς θετικών αποτελεσμάτων σε vH-SIL και ψευδώς αρνητικών σε dVIN2.
- Η αιδοιοσκόπηση κατά αναλογία της κολποσκόπησης, αναφέρεται από ιατρούς Μαιευτήρες – Γυναικολόγους1.
- Η δερματοσκόπηση αναφέρεται σε πρόσφατες μελέτες στη βιβλιογραφία ως χρήσιμο διαγνωστικό εργαλείο5.
- Η διάγνωση, όμως, τίθεται με την ιστολογική εξέταση και συχνά ειδικά σε πολυεστιακές βλάβες πρέπει να ληφθούν πολλαπλά δείγματα από διαφορετικά σημεία του προσβεβλημένου βλεννογόνου.
Το ιδανικό δείγμα βιοψίας θεωρείται ότι πρέπει να έχει ελάχιστο πλάτος 4 mm και βάθος 5 mm όταν πρόκειται για έντριχο δέρμα και 3 mm πλάτος και βάθος όταν λαμβάνεται από άτριχο δέρμα & βλεννογόνο1.
Ε. Ιστοπαθολογία – Ανοσοϊστοχημεία
Ε1. Υψηλού βαθμού πλακώδεις ενδοεπιθηλιακές βλάβες του αιδοίου (vH-SIL)
Ιστολογικά ταξινομούνται σε δύο διαφορετικούς υποτύπους: μυρμηκιώδεις και βασικοειδείς4. Συνήθως, η επιδερμίδα είναι παχυσμένη και συνοδεύεται από υπερκεράτωση ή/και παρακεράτωση. Υπάρχει απώλεια κυτταρικής ωρίμανσης με υπερχρωματικούς πυρήνες, πλειομορφισμό και πολυάριθμες μιτώσεις σε όλα τα επίπεδα της επιδερμίδας4.
Στις μυρμηκιώδεις vH-SIL η επιδερμίδα έχει ευρείες και βαθιές καταδύσεις, φτάνοντας συχνά κοντά στην επιφάνεια, γεγονός που δίνει μια χαρακτηριστική εμφάνιση. Επιπλέον, παρατηρούνται συχνά κοιλοκυττάρωση, δυσκεράτωση, πολυπύρηνα κύτταρα, ανώμαλες μιτώσεις και ακάνθωση4.
Οι βασικοειδείς vH-SIL χαρακτηρίζονται από παχυσμένο επιθήλιο με σχετικά επίπεδη και μη θηλωματώδη επιφάνεια. Στην επιδερμίδα παρατηρείται μεγάλος αριθμός σχετικά ομοιόμορφων αδιαφοροποίητων κυττάρων με βασικοειδή εμφάνιση. Οι μιτώσεις είναι πολυάριθμες, αλλά τα κοιλοκύτταρα και τα δυσκερατωσικά κύτταρα παρατηρούνται λιγότερο συχνά από ό,τι στις μυρμηκιώδεις vH-SIL. Συχνά στην ίδια βλάβη μπορεί να συνυπάρχουν ευρήματα μυρμηκιώδους και βασικοειδούς, και τότε χαρακτηρίζεται ως μικτή VIN4.
Η ανοσοϊστοχημεία με p16 μπορεί να είναι χρήσιμη στη διαφοροποίηση των VLSIL από τη VHSIL2. (Πίνακας 1)
Ε2. διαφοροποιημένη ενδοεπιθηλιακή νεοπλασία του αιδοίου (dVIN)
εύκολα συγχέεται με καλοήθεις δερματοπάθειες λόγω του υψηλού βαθμού κυτταρικής διαφοροποίησης και της απουσίας εκτεταμένης αρχιτεκτονικής αταξίας. Τα ιστολογικά χαρακτηριστικά της dVIN περιλαμβάνουν ένα παχυμένο επιθήλιο με παρακεράτωση, σπογγίωση, έλλειψη κοκκώδους στιβάδας, επιμήκεις και αναστομωτικές καταδύσεις και ευμεγέθη ανώμαλα κερατινοκύτταρα με πρόωρη ηωσινοφιλική κυτταροπλασματική διαφοροποίηση. Αυτά τα ανώμαλα κερατινοκύτταρα περιορίζονται στη βασική και παραβασική στιβάδα και αποτελούν χαρακτηριστικό γνώρισμα της dVIN2,4.
Η χρώση με MIB1 (Ki-67), έναν δείκτη που απεικονίζει τα πολλαπλασιαζόμενα κύτταρα, βοηθά στη διάκριση της dVIN από το φυσιολογικό επιθήλιο του αιδοίου. Η βασική στιβάδα στη dVIN είναι θετική για MIB1, ενώ το φυσιολογικό επιθήλιο του αιδοίου χαρακτηρίζεται από μία σχεδόν MIB1-αρνητική βασική στιβάδα. Ένα άλλο χρήσιμο εργαλείο είναι η χρώση για την πρωτεΐνη p53 γιατί η υπερέκφραση του p53 έχει αποδειχθεί στη dVIN4.
Τα ιστολογικά χαρακτηριστικά της dVIN μπορεί να μην είναι εύκολα διακριτά ειδικά όταν η ιστολογική εικόνα περιπλέκεται από υποκείμενες παθήσεις όπως ο σκληροατροφικός λειχήνας. Σύμφωνα με τους van de Nieuwenhof et al., το 42% των βιοψιών που αρχικά διαγνώστηκαν ως σκληροατροφικός λειχήνας ταξινομήθηκαν ως dVIN μετά από επανεξέταση2.
Στ. Θεραπεία Ενδοεπιθηλιακής Νεοπλασίας Αιδοίου (VIN)
Για τη θεραπεία της Ενδοεπιθηλιακής Νεοπλασίας Αιδοίου (VIN) υπάρχει έλλειψη τεκμηριωμένων (evidence – based) κριτηρίων και ασυμφωνία στη βιβλιογραφία.
Η θεραπεία υπαγορεύεται από τα:
- Χαρακτηριστικά της βλάβης: μέγεθος, θέση, πολυεστιακότητα, πιθανή διήθηση
- Χαρακτηριστικά της ασθενούς: ηλικία, συμπτώματα, συννοσηρότητες, αξιοπιστία παρακολούθησης
- Διαθεσιμότητα ιατρικών μέσων και εμπειρογνωμοσύνης
Ενώ οι στόχοι της θεραπείας είναι η:
- Πρόληψη εξέλιξης σε διηθητικό καρκίνο του αιδοίου
- Πρόληψη υποτροπής
- Ανακούφιση των συμπτωμάτων και η
- Διατήρηση της ανατομίας και της λειτουργικότητας του αιδοίου, και της ποιότητας ζωής1
ΣΧΗΜΑ 2. Γραφική παράσταση της θεραπείας για τη VIN.
Για την αποτελεσματική αντιμετώπιση των βλαβών του αιδοίου είναι σημαντική η εκπαίδευση, η υποστήριξη και η παροχή συμβουλών στις ασθενείς. Οι πληροφορίες θα πρέπει να παρέχονται γραπτώς μέσω φυλλαδίων, ιστοτόπων και γραπτών οδηγιών. Η χρήση καθρεφτών ή μοντέλων σε κλινικές βοηθά στην καθοδήγηση για τη σωστή εφαρμογή τοπικών θεραπειών. Η προστασία του φραγμού του δέρματος ή του βλεννογόνου στην περιοχή του αιδοίου περιλαμβάνει την αποφυγή ερεθιστικών ουσιών, όπως το σαπούνι, τη χρήση ειδικών καθαριστικών και ήπιων μαλακτικών για ενυδάτωση. Ο ερεθισμός που οφείλεται σε ακράτεια ούρων και κοπράνων θα πρέπει να αντιμετωπίζεται κατάλληλα ώστε να μην επιδεινώνεται περαιτέρω η υποκείμενη παθολογία του δέρματος. Τα τοπικά στεροειδή θα πρέπει να χρησιμοποιούνται για τη μείωση της φλεγμονής σε παθήσεις όπως ο ομαλός λειχήνας, ο σκληροατροφικός λειχήνας και το έκζεμα. Οι ασθενείς πρέπει να καθησυχάζονται σχετικά με τις παρενέργειες των τοπικών κορτικοστεροειδών. Είναι γνωστό ότι οι βλεννογόνοι, όπως η περιοχή του αιδοίου, είναι ανθεκτικοί στην ανάπτυξη ατροφίας εκ κορτικοειδών όταν εφαρμόζεται η σωστή ισχύς φαρμάκου με ελεγχόμενη διάρκεια και σωστή θέση εφαρμογής2.
Σύμφωνα με τις συστάσεις του 2016 για τη διαχείριση της vH-SIL που δημοσιεύθηκαν από το Αμερικανικό Κολέγιο Μαιευτήρων και Γυναικολόγων (ACOG) και την Αμερικανική Εταιρεία Κολποσκόπησης και Παθολογίας του Τραχήλου της Μήτρας, η vH-SIL μπορεί να αντιμετωπιστεί με χειρουργική εκτομή, αφαίρεση με λέιζερ ή τοπική ιμικουιμόδη όταν δεν υπάρχουν σημάδια λανθάνουσας διήθησης1.
Η χειρουργική θεραπεία ειδικά για νεαρές γυναίκες οι οποίες συχνά έχουν πολυεστιακές βλάβες, προκαλεί ακρωτηριασμό με σοβαρές ψυχοσεξουαλικές επιπτώσεις και έτσι σε μια ανασκόπηση του Cochrane το 2016 των ιατρικών και χειρουργικών παρεμβάσεων για τη θεραπεία της VIN, οι Lawrie et al συνέστησαν τη χειρουργική εκτομή ως θεραπεία δεύτερης γραμμής για ασθενείς που αποτυγχάνουν να ανταποκριθούν στην τοπική θεραπεία1,6.
1. Χειρουργική θεραπεία
Η κλασική θεραπεία για τις υψηλού βαθμού πλακώδεις ενδοεπιθηλιακές αλλοιώσεις του αιδοίου (vH-SIL), είναι η χειρουργική εκτομή και, στην περίπτωση πολυεστιακών βλαβών, η αιδοιοεκτομή. Οι ριζικές και συχνά ακρωτηριαστικές θεραπείες δε συνοδεύονται από αντίστοιχη επιτυχία με τα ποσοστά υποτροπής να κυμαίνονται μεταξύ 10% και 50%1.
Δεν υπάρχουν τεκμηριωμένες κατευθυντήριες γραμμές για το μέγεθος των πλευρικών υγιών ορίων κατά τη χειρουργική εκτομή της VIN. Αρκετοί συγγραφείς συμφωνούν ότι, ελλείψει διηθητικής νόσου, η επιφανειακή εκτομή του δέρματος με εν τω βάθει αφαίρεση 5 mm υποκείμενου λίπους και πλευρικά όρια τουλάχιστον 5 mm είναι επαρκής. Οι Ioffe et al συνιστούν παρακολούθηση και όχι επανεκτομή για ασθενείς με διήθηση των ορίων. Σύμφωνα με τους Jones et al, το 50% των γυναικών με θετικά όρια εκτομής θα χρειαστούν επανάληψη της θεραπείας έναντι 15% εκείνων με αρνητικά όρια1,7-8.
Για τη διαφοροποιημένη ενδοεπιθηλιακή νεοπλασία του αιδοίου (dVIN) η ευρωπαϊκή κατευθυντήρια γραμμή του 2016 για τη διαχείριση των παθήσεων του αιδοίου συστήνει ως θεραπεία εκλογής τη χειρουργική εκτομή. Η διάγνωση πρέπει πάντα να επιβεβαιώνεται με βιοψία, καθώς αυτές οι βλάβες μπορούν να εξελιχθούν σε διηθητικό ΑΚΚ1,9-10.
2. Λέιζερ
Η ευρωπαϊκή κατευθυντήρια γραμμή του 2016 περιγράφει τη θεραπεία με λέιζερ CO2 ως εναλλακτική λύση στη χειρουργική επέμβαση για vHSIL. Σε μια αναδρομική μελέτη 73 ασθενών με vH-SIL, δε βρέθηκαν διαφορές στην επιβίωση χωρίς υποτροπή μεταξύ των ασθενών που έλαβαν θεραπεία με λέιζερ CO2, χειρουργική εκτομή και ιμικουιμόδη1,6.
Η θεραπεία με λέιζερ CO2 πρέπει να εφαρμόζεται μόνο σε δέρμα που δεν φέρει τρίχες με επιφανειακό βάθος διείσδυσης 2 mm. Ένα μειονέκτημα της εξάχνωσης με λέιζερ είναι ότι προκαλεί μετεγχειρητικό πόνο και απαιτεί μεγαλύτερη φροντίδα τραύματος σε σχέση με τη χειρουργική επέμβαση1.
Η θεραπεία με λέιζερ CO2 μπορεί να θεωρηθεί ως εναλλακτική λύση στην ιμικιμόδη για vH-SIL χωρίς ιστολογικά σημεία λανθάνουσας διήθησης σε νεαρές γυναίκες για τις οποίες η χειρουργική εκτομή θα προκαλούσε παραμόρφωση των δομών. Η εξάχνωση με λέιζερ, ωστόσο, δεν συνιστάται για dVIN, καθώς δεν παρέχει δείγμα για ιστολογική εξέταση κάτι που είναι ιδιαίτερα σημαντικό λαμβάνοντας υπόψη το κακοήθες δυναμικό αυτών των βλαβών1.
3. Υπερηχητική Χειρουργική Αναρρόφηση (CUSA)
Η Υπερηχητική Χειρουργική Αναρρόφηση (CUSA) είναι μια πιο σύγχρονη τεχνική κατά την οποία υπερηχητικά κύματα διασπούν τον ιστό στο δικτυωτό χόριο που στη συνέχεια τον αναρροφούν. Θεωρείται ότι επιτυγχάνει επιλεκτική αφαίρεση πάσχοντος ιστού, εξοικονομεί υγιή περιβάλλοντα ιστό και παρέχει δείγμα που μπορεί να σταλεί για ιστολογική εξέταση. Η CUSA έχει δείξει υποσχόμενα αποτελέσματα σε αρκετές μελέτες, συμπεριλαμβανομένης μιας τυχαιοποιημένης κλινικής δοκιμής (RCT) από τους Von Gruenigen et al στην οποία συγκρίθηκε με τη θεραπεία με λέιζερ CO2 με παρόμοια ποσοστά υποτροπής σε ένα έτος που κυμαίνονται από 22%-35%11. Στο RCT του Von Gruenigen, οι ασθενείς στο σκέλος CUSA είχαν σημαντικά λιγότερες μετεγχειρητικές ανεπιθύμητες ενέργειες και μικρότερη ουλοποίηση από εκείνες που είχαν υποβληθεί σε λέιζερ. Οι Miller et al. έδειξαν σε μια αναδρομική μελέτη ότι η υποτροπή ήταν σημαντικά συχνότερη για τους σχετιζόμενους με VIN έντριχους ιστούς (p=0,04) και επομένως αυτή η θεραπεία, όπως και το λέιζερ, δεν πρέπει να χρησιμοποιείται σε έντριχους ιστούς1,11-12.
4. Τοπική θεραπεία
4α. Ιμικουϊμόδη (Imiquimod). Η ιμικουϊμόδη (Imiquimod) είναι ένας τοπικός ανοσοτροποποιητής που δεν έχει άμεση αντιική δράση αλλά δρα επάγοντας τοπική in vivo ανοσολογική απόκριση στοχεύοντας κύτταρα μολυσμένα με HPV13.
Η ιμικιμόδη έχει εγκριθεί για τη θεραπεία των HPV γεννητικών και περιπρωκτικών κονδυλωμάτων, αλλά όχι για τη VIN. Παρόλο που η ιμικουιμόδη δεν ενδείκνυται για τη θεραπεία της vH-SIL, τόσο οι κατευθυντήριες οδηγίες των ΗΠΑ όσο και της Ευρώπης τη συνιστούν ως θεραπεία πρώτης γραμμής και προτείνουν να ακολουθείται από χειρουργική εκτομή σε ασθενείς που δεν ανταποκρίνονται ή σε ασθενείς με υπολειμματική ή εξελισσόμενη νόσο12,14.
Σε σύγκριση με την πιο επιθετική επιλογή της χειρουργικής εκτομής, είναι μια ιδιαίτερα ενδιαφέρουσα επιλογή καθώς οι βλάβες vH-SIL είναι συχνά πολυεστιακές και οι ακρωτηριαστικές χειρουργικές επεμβάσεις επηρεάζουν ψυχολογικά τις νέες γυναίκες1.
Το δοσολογικό σχήμα που συνιστάται από την ACOG είναι εφαρμογή τρεις φορές την εβδομάδα στις πάσχουσες περιοχές για 12 έως 20 εβδομάδες με αιδοιοσκοπική αξιολόγηση κάθε 4 έως 6 εβδομάδες κατά τη διάρκεια της θεραπείας14.
Δύο τυχαιοποιημένες ελεγχόμενες μελέτες συνέκριναν την ιμικουϊμόδη με εικονικό φάρμακο στο 87% των ασθενών που συμμετείχαν σε πιλοτική μελέτη με πλήρη ή μερική ανταπόκριση. 2 και 5 μήνες μετά τη θεραπεία, οι Mathiesen et al. και van Seters et al. ανέφεραν ποσοστό πλήρους ανταπόκρισης 81% και 35%, αντίστοιχα, μεταξύ των γυναικών που έλαβαν θεραπεία με ιμικουιμόδη15,16. Σε περίοδο παρακολούθησης 12 μηνών, οι van Seters et al. δεν βρήκαν διαφορά στα ποσοστά εξέλιξης σε διηθητική νόσο μεταξύ των δύο ομάδων (1/26 έναντι 2/26), με 35% των ασθενών που ανταποκρίθηκαν πλήρως (n=9) στην ομάδα της ιμικουιμόδης και 0% στην ομάδα του εικονικού φαρμάκου16. Μετά από διάμεσο χρόνο παρακολούθησης 7,2 ετών, οκτώ από τους εννέα αρχικούς ασθενείς που ανταποκρίθηκαν πλήρως παρέμειναν απαλλαγμένοι από τη νόσο15,16.
Οι τοπικές ανεπιθύμητες ενέργειες της θεραπείας με ιμικουϊμόδη περιλαμβάνουν αίσθημα καύσους μετά την εφαρμογή, πόνο, ερύθημα, διάβρωση, οίδημα, κνησμό και γενικές αντιδράσεις όπως κεφαλαλγία, απάθεια, εξασθένιση και μυαλγία17. Αυτές οι επιδράσεις έχουν συχνά ως αποτέλεσμα την κακή συμμόρφωση και πρόωρη διακοπή της θεραπείας. Λίγες μελέτες έχουν αναλύσει τις μακροπρόθεσμες επιδράσεις της ιμικουϊμόδης και οι περισσότερες από αυτές ήταν μικρές σειρές με σύντομους χρόνους παρακολούθησης1.
Μια ολλανδική ομάδα με επικεφαλής τους Terlou et al ανέλυσε τις μακροπρόθεσμες επιδράσεις της θεραπείας σε ασθενείς που έλαβαν θεραπεία με ιμικουϊμόδη στο RCT από τους Van Seters et al (n = 26)16,17. Οκτώ από τους εννέα ασθενείς που είχαν δείξει πλήρη ανταπόκριση μετά από 20 εβδομάδες θεραπείας παρέμειναν ελεύθεροι νόσου στα 5 έτη και δεν είχαν δείξει σημεία υποτροπής. Η ανασκόπηση Cochrane του 2016 της ιατρικής και χειρουργικής θεραπείας του vH-SIL από τους Lawrie et al διαπίστωσε ότι οι μικρές βλάβες ήταν προγνωστικός δείκτης καλής ανταπόκρισης στην ιμικουϊμόδη, ενώ οι πολυεστιακές βλάβες ήταν παράγοντας κινδύνου υποτροπής1,6.
Καμία μελέτη δεν έχει αναλύσει την ιμικουϊμόδη στη θεραπεία της dVIN, αν και έχει διερευνηθεί σε μελέτες και συνεχιζόμενες δοκιμές για το βασικοκυτταρικό καρκίνωμα και τη νόσο Paget. Ωστόσο, αναφορές στη βιβλιογραφία φαίνεται να δείχνουν ότι η ιμικουϊμόδη είναι λιγότερο αποτελεσματική σε βλάβες ανεξάρτητες από τους ιούς HPV1.
4β. Σιντοφοβίρη (cidofovir). Η τοπική κρέμα Σιντοφοβίρης (cidofovir 1%) είναι ένα νουκλεοτιδικό ανάλογο της κυτοσίνης που αναστέλλει την αντιγραφή των ιών HPV αναστέλλοντας τις πολυμεράσες του ιικού DNA. Έχει χορηγηθεί προσωρινή άδεια για χρήση στη VIN στη Γαλλία1.
Η σιντοφοβίρη και η ιμικουϊμόδη συγκρίθηκαν σε μια δοκιμή φάσης 2 ασθενών με VIN 3 στο Ηνωμένο Βασίλειο. Η εφαρμογή έγινε τρεις φορές εβδομαδιαίως για μέγιστο διάστημα 12 εβδομάδων. Δεν υπήρξε διαφορά στα ποσοστά πλήρους ανταπόκρισης (περίπου 46%) μεταξύ των ομάδων μετά από 6 μήνες θεραπείας. Σε 12 μήνες παρακολούθησης, τα ποσοστά πλήρους ανταπόκρισης ήταν 87% για τη cidofovir και 78% για την ιμικουϊμόδη. Η συχνότητα των ανεπιθύμητων ενεργειών ήταν παρόμοια στις δύο ομάδες, εκτός από την κόπωση και την κεφαλαλγία, οι οποίες ήταν πιο συχνές σε ασθενείς που έλαβαν θεραπεία με ιμικουϊμόδη18.
4γ. Φωτοδυναμική θεραπεία (PDT). Η φωτοδυναμική θεραπεία (PDT) έχει χρησιμοποιηθεί για τη θεραπεία πολλών παθολογικών καταστάσεων του δέρματος και των βλεννογόνων.
Οι μελέτες που έχουν αναλύσει τη PDT στη θεραπεία της VIN έχουν χρησιμοποιήσει διαφορετικές μεθοδολογίες και τα ευρήματά τους στηρίζονται σε χαμηλό αποδεικτικό επίπεδο. Σε μια βιβλιογραφική ανασκόπηση για το ρόλο της PDT στη θεραπεία της vH-SIL που δημοσιεύθηκε το 2018, η ιταλική ομάδα με επικεφαλής τους Tosti et al ανέφερε ποσοστά πλήρους ιστολογικής ανταπόκρισης που κυμαίνονται από 20% έως 67% και ποσοστά ανακούφισης συμπτωμάτων από 52% έως 89%1,19.
Τα ευρήματά τους, ωστόσο, έδειξαν ότι οι πολυεστιακές βλάβες ήταν πολύ πιο δύσκολο να αντιμετωπιστούν, καθώς μόνο το 27% αυτών των ασθενών πέτυχαν πλήρη ύφεση1,19.
4δ. Ινδολο-3-καρβινόλη (I3C). Η Ινδολο-3-καρβινόλη (I3C) είναι μια φυσική ένωση που υπάρχει σε μεγάλες συγκεντρώσεις σε σταυρανθή λαχανικά. Μία μικρή τυχαιοποιημένη ελεγχόμενη μελέτη (randomized controlled trial RCT), που δημοσιεύθηκε το 2006 συνέκρινε την αποτελεσματικότητα δύο δόσεων I3C για τη θεραπεία της vH-SIL. Η ανασκόπηση Cochrane που δημοσιεύθηκε από τους Pepas et al το 2015 κατέληξε στο συμπέρασμα ότι η δοκιμή δεν απέδειξε την αποτελεσματικότητα της ένωσης αυτής1,20.
5. Θεραπευτικός εμβολιασμός
Στόχος του θεραπευτικού εμβολιασμού είναι η ενίσχυση των ειδικών για τον HPV αποκρίσεων των CD4+ και CD8+ Τ κυττάρων σε βλάβες vH-SIL. Τα περισσότερα εμβόλια επάγουν ειδική ανοσία έναντι των ογκογόνων πρωτεϊνών Ε6 και Ε7 των ιών HPV. Δύο μελέτες ανέλυσαν την αποτελεσματικότητα ενός συνδυασμού δύο εμβολίων (TA-HPV και TA-CIN) σε γυναίκες με vH-SIL σχετιζόμενο με HPV 16. Από τις 39 ασθενείς που έλαβαν θεραπεία, εννέα ασθενείς παρουσίασαν συρρίκνωση βλαβών, 25 παρέμειναν σταθερές και πέντε εμφάνισαν εξέλιξη της νόσου. Το συνδυασμένο θεραπευτικό εμβόλιο αποδείχθηκε ανοσογόνο αλλά δεν παρατηρήθηκε συσχέτιση μεταξύ της επαγόμενης ειδικής ανοσίας έναντι των HPV και των κλινικών αποτελεσμάτων1,21-22.
Τα θεραπευτικά εμβόλια βρίσκονται ακόμη στο στάδιο της έρευνας και δίνεται περισσότερη έμφαση στην πρόληψη μέσω του εμβολιασμού1.
6. Παρακολούθηση χωρίς θεραπεία
Η ευρωπαϊκή κατευθυντήρια γραμμή του 2016 προτείνει την παρακολούθηση χωρίς θεραπεία ως εναλλακτική λύση στην τοπική ή χειρουργική αντιμετώπιση της vH-SIL12. Στη βιβλιογραφία αναφέρονται περιστατικά αυτόματης υποστροφής ιδιαίτερα μεταξύ νεαρών ασθενών8. Ωστόσο, η αυτόματη ύφεση δεν μπορεί να προβλεφθεί και, ως εκ τούτου, συνιστάται στενή παρακολούθηση σε ασθενείς που δεν λαμβάνουν θεραπεία1.
Ζ. Πρόληψη
Η πρόληψη για τις σχετιζόμενες με τους ιούς HPV, ενδοεπιθηλιακές νεοπλασίες του αιδοίου (vL-SIL και vHSIL) βασίζεται στον εμβολιασμό έναντι των ιών HPV σε νεαρή ηλικία.
Στην Ελλάδα διατίθενται σήμερα δύο HPV εμβόλια, το διδύναμο (HPV2) και το εννεαδύναμο (HPV9).
Η Εθνική Επιτροπή Εμβολιασμών προτείνει ως ηλικία έναρξης του εμβολιασμού έναντι του HPV τα εννέα (9) έτη με στόχο (α) τη διασφάλιση της βέλτιστης δυνατής ανοσολογικής απάντησης από τον εμβολιασμό και (β) την κατά το δυνατό έγκαιρη προστασία από την έκθεση στον ιό HPV. Σε περίπτωση που ο εμβολιασμός δεν διενεργηθεί στη συνιστώμενη ηλικία (9-11 ετών), η Επιτροπή επισημαίνει ότι θα πρέπει να πραγματοποιηθεί το συντομότερο δυνατό23.
Και τα δύο εμβόλια χορηγούνται σε 2 δόσεις με μεσοδιάστημα 6 μηνών (σχήμα 0,6). Σε περίπτωση που οι 2 δόσεις γίνουν σε μεσοδιάστημα μικρότερο των 5 μηνών, απαιτείται και 3η δόση 6 μήνες μετά την πρώτη δόση και τουλάχιστον 3 μήνες μετά την 2η δόση. Εφόσον η έναρξη του HPV εμβολιασμού γίνει μετά την συμπλήρωση του 15ου έτους της ηλικίας, χορηγούνται 3 δόσεις εμβολίου ως εξής: Αρχικά η πρώτη δόση, μετά 1 μήνα (για το διδύναμο εμβόλιο) ή μετά 2 μήνες (για το εννεαδύναμο εμβόλιο) γίνεται η δεύτερη δόση και μετά 6 μήνες από την 1η δόση γίνεται η 3η δόση23.
Το HPV εμβόλιο συνιστάται στις γυναίκες 18-26 ετών (σε τρεις δόσεις, σχήμα: 0, 1-2, 6). Δεν συνιστάται σε έγκυες γυναίκες, ωστόσο δεν είναι απαραίτητο να γίνεται τεστ εγκυμοσύνης πριν την έναρξη του εμβολιασμού. Εάν διαπιστωθεί ότι μια γυναίκα είναι έγκυος μετά την έναρξη του εμβολιασμού, δεν συνιστάται διακοπή της κύησης και οι υπόλοιπες δόσεις συμπληρώνονται μετά την ολοκλήρωση της κύησης. Ο HPV εμβολιασμός συνιστάται επίσης σε γυναίκες με νεφρική ανεπάρκεια τελικού σταδίου με αιμοδιάλυση, με χρόνια νοσήματα όπως σακχαρώδη διαβήτη, καρδιακή νόσο, πνευμονοπάθεια, ρευματικά νοσήματα, αλκοολισμό, ασπληνία, ανεπάρκεια κλασμάτων συμπλέγματος, χρόνια ηπατική νόσο. Επίσης, ο HPV εμβολιασμός συνιστάται στην Ελλάδα και σε άνδρες μέχρι 26 ετών, οι οποίοι έχουν σεξουαλικές επαφές με άνδρες, για την πρόληψη του καρκίνου του πρωκτού.
Καταστάσεις ανοσοκαταστολής για τις οποίες απαιτείται δοσολογικό σχήμα 3 δόσεων είναι οι πρωτοπαθείς ή δευτεροπαθείς ανοσοανεπάρκειες που οδηγούν σε μείωση της κυτταρικής ή χυμικής ανοσίας23.
Σε μια μελέτη της επίδρασης του προφυλακτικού εμβολιασμού έναντι των HPV τύπων 11, 16 και 18 στη σχετιζόμενη με HPV ενδοεπιθηλιακή νεοπλασία των γεννητικών οργάνων σε γυναίκες, οι Muñoz et al έδειξαν αποτελεσματικότητα 94,9% σε γυναίκες που δεν είχαν ποτέ μολυνθεί από HPV και 75,6% σε μια μικτή ομάδα γυναικών που εκτέθηκαν σε HPV και δεν εκτέθηκαν (ομάδα πρόθεσης για θεραπεία). Η μείωση της συχνότητας εμφάνισης vH-SIL μεταξύ εμβολιασμένων ασθενών είναι πιθανό να μειώσει τη συχνότητα εμφάνισης καρκίνου του αιδοίου1,15,24.
Η. Παρακολούθηση
Σύμφωνα με το Αμερικάνικο Κολέγιο Μαιευτήρων – Γυναικολόγων (ACOG – American College of Obstetricians and Gynecologists), οι γυναίκες με πλήρη ανταπόκριση στη θεραπεία εκτιμώνται σε προγραμματισμένες επισκέψεις παρακολούθησης 6 μήνες και 12 μήνες μετά την αρχική θεραπεία. Αν σε αυτές τις επισκέψεις δεν παρατηρηθούν νέες αλλοιώσεις συστήνεται να παρακολουθούνται με κλινική εξέταση του αιδοίου ετησίως στη συνέχεια14.
Η ευρωπαϊκή κατευθυντήρια γραμμή του 2016 συστήνει μια εξέταση παρακολούθησης κάθε 6 έως 12 μήνες με ετήσιο τραχηλικό επίχρισμα για ασθενείς με vH-SIL και κάθε 6 μήνες για εκείνους με dVIN12.
Η μακροχρόνια παρακολούθηση, συμπεριλαμβανομένης της εξέτασης του αιδοίου και γενικά της πρωκτογεννητικής περιοχής, είναι απαραίτητη, δεδομένου ότι πάνω από το 25% των ασθενών εμφανίζουν καθυστερημένη υποτροπή1,25.
BIBΛΙΟΓΡΑΦΙΑ
- Lebreton M., Carton I., Brousse S., et al. Vulvar intraepithelial neoplasia: classification, epidemiology, diagnosis, and management. J Gynecol Obstet Hum Reprod. 2020 Nov;49(9):101801 doi: 10.1016/j.jogoh.2020.101801. Epub 2020 May 14.
- Gupta S., Ahuja S, Kalwaniya, Shamsunder S, Solanki, S. Vulval premalignant lesions: a review article. Obstet Gynecol Sci 2024;67(2):169-185. doi: 10.5468/ogs.23274. Epub 2024 Jan 23.
- Sarbu MI, Sarbu IF, Tampa M, et al. Buschke-Löwenstein tumor of the vulva in a patient with a history of squamous cell carcinoma of the cervix. BMC Infectious Diseases 2014, 14(Suppl 7):P11. doi: 10.1186/1471-2334-14-S7-P11
- Terlou A, Blok LJ, Helmerhorst TJM, van Beurden M. Premalignant epithelial disorders of the vulva: squamous vulvar intraepithelial neoplasia, vulvar Paget’s disease and melanoma in situ. Acta Obstet Gynecol Scand. 2010 Jun;89(6):741-8. doi: 10.3109/00016341003739575.
- De Giorgi V, Magnaterra E, Zuccaro B, et al. Assessment of Vulvar Intraepithelial Neoplasia (VIN) Grades Based on Dermoscopic Features: A Diagnostic Study. Dermatol Pract Concept. 2023 Oct 1;13(4):e2023269. doi: 10.5826/dpc.1304a269
- Lawrie TA, Nordin A, Chakrabarti M, Bryant A, Kaushik S, Pepas L. Medical and surgical interventions for the treatment of usual-type vulval intraepithelial neoplasia. Cochrane Database Syst Rev 2016:CD011837.
- Ioffe YJ, Erickson BK, Foster KE, et al. Low yield of residual vulvar carcinoma and dysplasia upon re-excision for close or positive margins. Gynecol Oncol 2013;129:528–32. https://doi.org/10.1016/j.ygyno.2013.02.033.
- Jones RW, Rowan DM, Stewart AW. Vulvar intraepithelial neoplasia: aspects of the natural history and outcome in 405 women. Obstet Gynecol 2005;106:1319–26.
- Preti M, Scurry J, Marchitelli CE, Micheletti L. Vulvar intraepithelial neoplasia. Best Pract Res Clin Obstet Gynaecol 2014;28:1051–62.https://doi.org/10.1016/j.bpobgyn.2014.07.010.
- van der Meijden WI, Boffa MJ, Ter Harmsel WA, et al. 2016 European guideline for the management of vulval conditions. J Eur Acad Dermatol Venereol 2017;31:925–41. https://doi.org/10.1111/jdv.14096.
- von Gruenigen VE, Gibbons HE, Gibbins K, Jenison EL, Hopkins MP. Surgical treatments for vulvar and vaginal dysplasia: a randomized controlled trial. Obstet Gynecol 2007;109:942–7. https://doi.org/10.1097/01.AOG.0000258783.49564.5c.
- Miller BE. Vulvar intraepithelial neoplasia treated with cavitational ultrasonic surgical aspiration. Gynecol Oncol 2002;85:114–8. https://doi.org/10.1006/gyno.2001.6577.
- de Witte CJ, van de Sande AJM, van Beekhuizen HJ, Koeneman MM, Kruse AJ, Gerestein CG. Imiquimod in cervical, vaginal and vulvar intraepithelial neoplasia: a review. Gynecol Oncol 2015;139:377–84. https://doi.org/10.1016/j.ygyno.2015.08.018.
- American College of Obstetricians and Gynecologists’ Committee on Gynecologic Practice, American Society for Colposcopy and Cervical Pathology (ASCCP). Committee Opinion No.675: Management of Vulvar Intraepithelial Neoplasia. Obstet Gynecol 2016;128:e178-182. https://doi.org/10.1097/AOG.0000000000001713.
- Mathiesen O, Buus SK, Cramers M. Topical imiquimod can reverse vulvar intraepithelial neoplasia: a randomised, double-blinded study. Gynecol Oncol 2007;107:219–22. https://doi.org/10.1016/j.ygyno.2007.06.003.
- Terlou A, van Seters M, Ewing PC, et al. Treatment of vulvar intraepithelial neoplasia with topical imiquimod: seven years median follow-up of a randomized clinical trial. Gynecol Oncol 2011;121:157–62. https://doi.org/10.1016/j.ygyno.2010.12.340.
- van Seters M, van Beurden M, ten Kate FJW, et al. Treatment of vulvar intraepithelial neoplasia with topical imiquimod. N Engl J Med 2008;358:1465–73. https://doi.org/10.1056/NEJMoa072685.
- Tristram A, Hurt CN, Madden T, et al. Activity, safety, and feasibility of cidofovir and imiquimod for treatment of vulval intraepithelial neoplasia (RT3VIN): a multicentre, open-label, randomised, phase 2 trial. The Lancet Oncology 2014;15:1361–8. https://doi.org/10.1016/S1470-2045(14)70456-5.
- Tosti G, Iacobone AD, Preti EP, et al. The Role of Photodynamic Therapy in the Treatment of Vulvar Intraepithelial Neoplasia. Biomedicines 2018;6. https://doi.org/10.3390/biomedicines6010013.
- Pepas L, Kaushik S, Nordin A, Bryant A, Lawrie TA. Medical interventions for highgrade vulval intraepithelial neoplasia. Cochrane Database Syst Rev 2015:CD007924. https://doi.org/10.1002/14651858.CD007924.pub3.
- Smyth LJC, Van Poelgeest MIE, Davidson EJ, et al. Immunological responses in women with human papillomavirus type 16 (HPV-16)associated anogenital intraepithelial neoplasia induced by heterologous prime-boost HPV-16 oncogene vaccination. Clin Cancer Res 2004;10:2954–61. https://doi.org/10.1158/1078-0432.ccr-03-0703.
- Davidson EJ, Faulkner RL, Sehr P, et al. Effect of TACIN (HPV 16 L2E6E7) booster immunisation in vulval intraepithelial neoplasia patients previously vaccinated with TA-HPV (vaccinia virus encoding HPV 16/18 E6E7). Vaccine 2004;22:2722–9. https://doi.org/10.1016/j.vaccine.2004.01.049.
- Σύσταση της Εθνικής Επιτροπής Εμβολιασμών για τον εμβολιασμό αγοριών και κοριτσιών έναντι του ιού των ανθρωπίνων θηλωμάτων 7. https://vaccineschedule. ecdc.europa.eu/ Scheduler/ ByDisease?Selected DiseaseId=38& SelectedCountry Id ByDisease=-1
- Muñoz N, Kjaer SK, Sigurdsson K, et al. Impact of human papillomavirus (HPV)-6/11/16/18 vaccine on all HPV-associated genital diseases in young women. J Natl Cancer Inst 2010;102:325–39. https://doi.org/10.1093/jnci/djp534.
- Satmary W, Holschneider CH, Brunette LL, Natarajan S. Vulvar intraepithelial neoplasia: Risk factors for recurrence. Gynecol Oncol 2018;148:126–31. https://doi.org/10.1016/j.ygyno.2017.10.029.